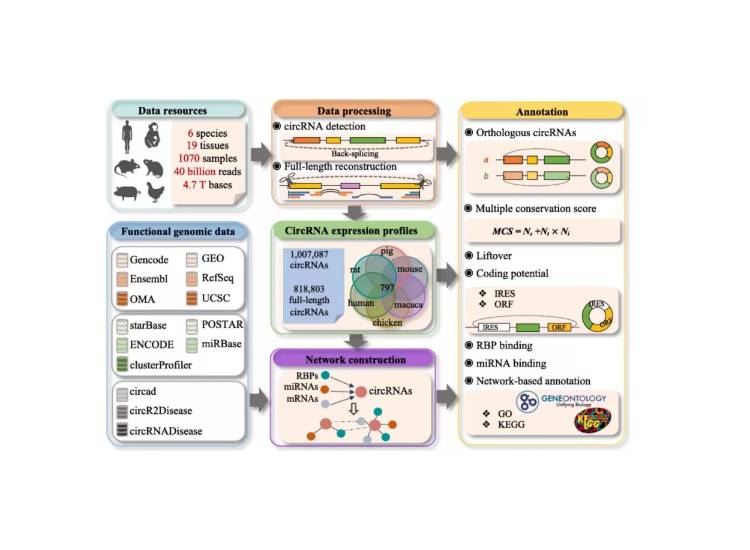
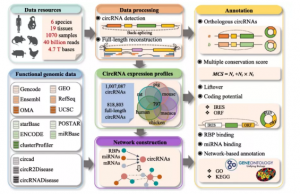
現有的環狀RNA (circRNA)數據庫已經成為轉錄組學的基礎。但是目前常用的方法對于深度挖掘候選circRNA仍有限。基于這種情況,趙方慶教授團隊2020年在genome biology雜志發表了circAtlas數據庫的文章(CircAtlas: an integrated resource of one million highly accurate circular RNAs from 1070 vertebrate transcriptomes)。circAtlas數據庫基于從六個脊椎動物物種(人類,獼猴,小鼠,大鼠,豬和雞)的19個正常組織中收集的1070個RNA-seq樣本數據匯總了環狀RNA相關信息。該數據庫包含1,007,087個高度可靠的circRNA,其中81.3%以上已被組裝成全長序列。數據庫終不僅概述了它們的表達模式、保守性和功能注釋等信息,還描述了一種新的多重保護評分、共表達和調控網絡,用于circRNA注釋和排序。
百邁客基于CircAtlas數據庫在已知circRNA鑒定上開發了新的流程,在原有的circBase數據庫上同時增加了本數據庫中包含物種的circRNA信息,讓已知circRNA鑒定的結果更加完善,更加豐富。
案例應用
案例一:位點保守的環狀RNAcZNF292控制內皮細胞流動反應
英文標題:Locus-Conserved Circular RNA cZNF292 Controls Endothelial Cell Flow Responses
雜志:Circ Res
影響因子:17.367
背景:環狀RNAs(CircRNAs)是由大多數mRNAs的反向剪接產生的,作為一類控制各種細胞功能的新型調節性RNAs,正受到越來越多的關注。然而,鑒于其基因失活的固有挑戰,它們在體內的生理作用和功能保護很少得到解決。在這里,我們的目的是在小鼠和人類中鑒定位點保守的CircRNAs,這些CircRNAs由于保留了mRNA宿主基因中不包含的內含子元件而被遺傳刪除,從而最終解決功能保守問題。
結果:作者通過RNA親和純化和隨后的質譜分析鑒定了與內皮細胞中cZNF292特異性相互作用的蛋白連接體(SDOS)。SDOS或其蛋白結合伙伴Syndecan-4的沉默,或SDOS-cZNF292結合位點的突變,阻止層流誘導的細胞骨架重組,從而重現cZfp292表型。結合已發表的內皮細胞RNA測序數據集和circATLAS數據庫的CircRNAs,作者在小鼠和人類之間鑒定了保留內含子元件的位點保守的CircRNA。CRISPR/Cas9介導的頂端表達的CircRNA cZfp292基因缺失導致體內主動脈內皮細胞形態改變和血流排列異常。體外內皮細胞中cZNF292的缺失消除了層流誘導的細胞定向、帕西林定位和粘著組織的改變。
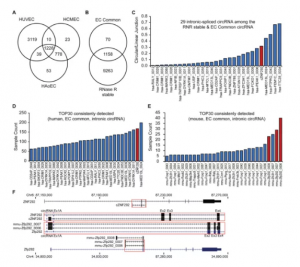
內含子circRNA篩選
案例二:環狀RNACircRHOBTB3通過調節HUR介導的PTBP1穩定性抑制結直腸癌轉移
標題:Circular RNA circRHOBTB3 represses metastasis by regulating the HuR-mediated mRNA stability of PTBP1 in colorectal cancer
雜志:Theranostic
影響因子:11.554
背景:結直腸癌(CRC)的腫瘤轉移是大多數患者死亡的主要原因,也是CRC綜合治療的主要難點。環狀RNA(CircRNA)影響實體瘤中的許多生物學功能。然而,它們在結直腸癌轉移中的作用機制尚不清楚
結果:作者發現circRHOBTB3在CRC組織和細胞系中表達明顯下調。此外,較低的circRHOBTB3水平與晚期臨床分期和更高的轉移風險顯著相關。circRHOBTB3過表達抑制結直腸癌細胞的腫瘤轉移。在機制上,circRHOBTB3結合于HuR (CRC發展中普遍表達的功能性RNA結合蛋白(RBP)),并促進β- trcp1介導的HuR泛素化。正常情況下,HuR與靶mRNA的3’UTR結合以促進其穩定,而circRHOBTB3和HuR的相互作用使HuR降低,從而降低下游靶蛋白PTBP1的表達水平。此外,在體內過表達的circRHOBTB3抑制肺轉移,而這種作用可以通過PTBP1的過表達部分逆轉。此外,FUS和ADARB2均可提高CRC細胞中circRHOBTB3的轉錄。其中,為了探索circRHOBTB3在CRC轉移的調控機制,作者首先篩選來自catRAPID,circAtlas,starBase和RBPDB檢索到的circRHOBTB3潛在的結合蛋白。根據結果,富含絲氨酸的剪接因子1(SRSF1)、FUS 和 HuR 可能與circRHOBTB3相互作用,然后使用生物素標記的探針circRHOBTB3進行RNA pulldown測定,結果證實circRHOBTB3可以與HuR互作但不與FUS互作,同時RIP分析也證實circRHOBTB3和HuR的相互作用。并且,為了更深入地了解circRHOBTB3的作用,作者根據 circAtlas數據庫,FUS可能與位于circRHOBTB3環化外顯子側翼的內含子結合。有趣的是,結果表明,沉默FUS強烈地抑制了circRHOBTB3的表達。
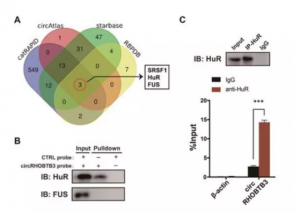
CircRHOBTB3潛在結合蛋白鑒定
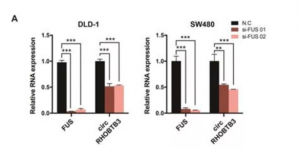
沉默FUS抑制CircRHOBTB3的表達
日前,百邁客云平臺(http://www.biocloud.net/)已經上線了CircRNA的個性化交互分析功能,完善的云服務模式深度助力提升客戶體驗,期待您的體驗,詳情請點擊下面鏈接跳轉查看~






 京公網安備 11011302003368號
京公網安備 11011302003368號